WBCの興奮が冷めない中で、日本のプロ野球、大リーグの試合が始まった。大谷選手の与えた衝撃は凄まじいものだった。それだけではなく、侍Japanの選手一人ひとりの能力、世界一に日本のチームを導いた礎にある、日本人の遺伝子にも驚愕した。

Smokingの研究から、その行為で傷ついた遺伝子は、孫の代まで影響を与えることが知られている。また、努力と経験で獲得した能力は、親から子へ、子から孫へと伝えられる。それがepigeneticsの働きだ。大谷選手の子供や孫にどんな遺伝子が残されるのか、とても興味深い。
4月号の原稿を書いていた時なので、ダルビッシュ選手が侍Japanの投手に投球方法を伝授している様子を見ていて、私はshort-rang quorum sensingのことを思っていた。
大腸菌が元々病原性大腸菌であったわけではないことは4月号で説明した。細菌の世界で生き残るために、戦士として鍛えられ、盾と剣を与えられた彼らは、巧妙なシステムを使って動物やヒトの免疫をかい潜り、今でもその能力を発揮して生き続けている。
モンサントは牛のミルクを大量生産するために、コーンを飼料として使った。家畜を製品として管理するためだった。そして、病原性大腸菌O-157は、その牛の胃の中で生まれた。彼らが獲得した毒素は、クオラムセンシングにより他の大腸菌に水平伝播し、彼らを変えていった。大腸菌の複製速度は20分で2倍になるので、2時間で64倍。1mmの1000分の1の大きさの大腸菌が、1日経つと1000億の100億倍の数に増えて、その体積はコップ1杯に相当する。もう1日おくと山の様な大きさになる。瞬く間に世界に広がっていったのはその爆発的な増植力の故だ。
病原性大腸菌
大腸菌は温血動物の腸管でみられ、病原性因子をコードする遺伝的要素を獲得しない限り良性であり、ヒトとの共生関係を維持している。経膣分娩により、母親の糞便を介して、出生後40時間以内に赤ちゃんの腸間でコロニーを形成する。ヒトの場合、異所感染として尿路系や血液中に侵入した場合に病原体となる。内毒素を産生するため、大腸菌による敗血症はエンドトキシンショックを引き起こす。大腸菌の株の中でも特に強い病原性を示すものは病原性大腸菌と呼ばれる。
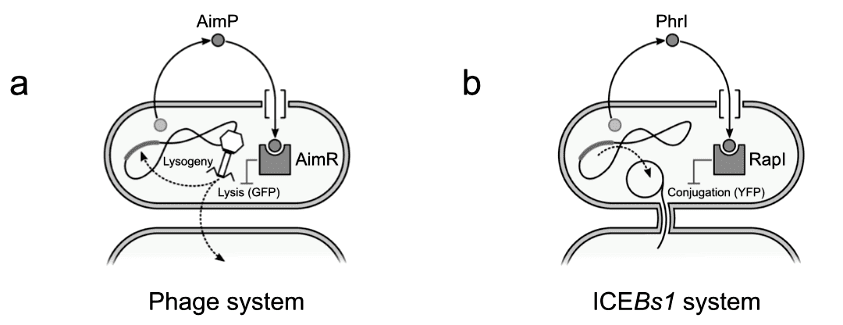
Quorum-sensing systems of(a)phage system(φ3T)and(b)integrative conjugative element(ICEBs1).
4月号でも書いたが、大腸菌及び多くの関連する細菌は、細菌接合(bacterial conjugation)や形質導入を介してDNAを転移する能力を持っており、これによって遺伝物質を既存の集団全体に水平的に広げることができる(遺伝子の水平伝播)。例えば志賀毒素をコードする遺伝子は、バクテリオファージと呼ばれるバクテリアウィルスを介した形質導入プロセスを通じて、赤痢菌から大腸菌に広がり、志賀毒素を持つ大腸菌O-157:H7が生まれたと考えられている。臨床医学上は赤痢菌がより重篤な病態を引き起こすことから、大腸菌とは異なる分類とされているが、近年の遺伝子に基づく分類学上では、赤痢菌と大腸菌は同種という位置づけになっているようだ。
感染する手立て
尿路感染性大腸菌(UPEC)は、下の図のように、付着因子(adhesins)、毒素(toxins)、鉄獲得因子、リポ多糖(LPS)、バイオフィルム の形成を助けるアミロイド繊維(Curli)、カプセルなど、その病因に寄与する毒性因子を持っている。
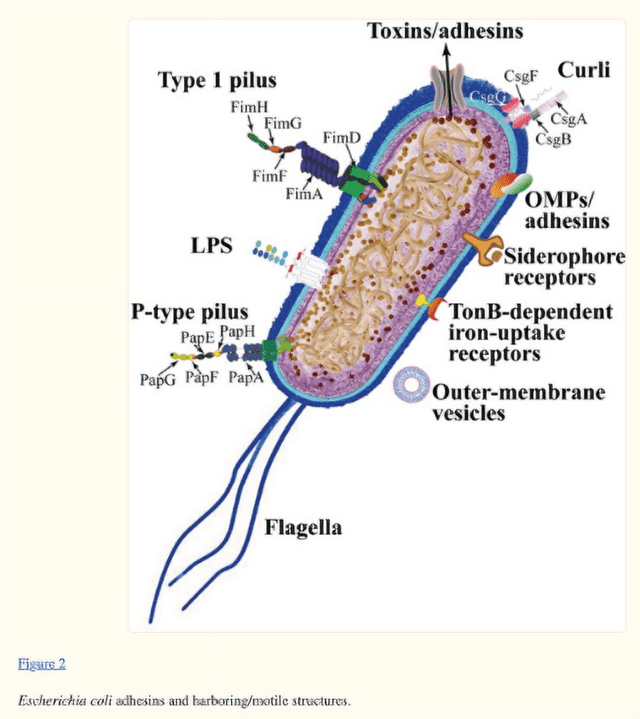
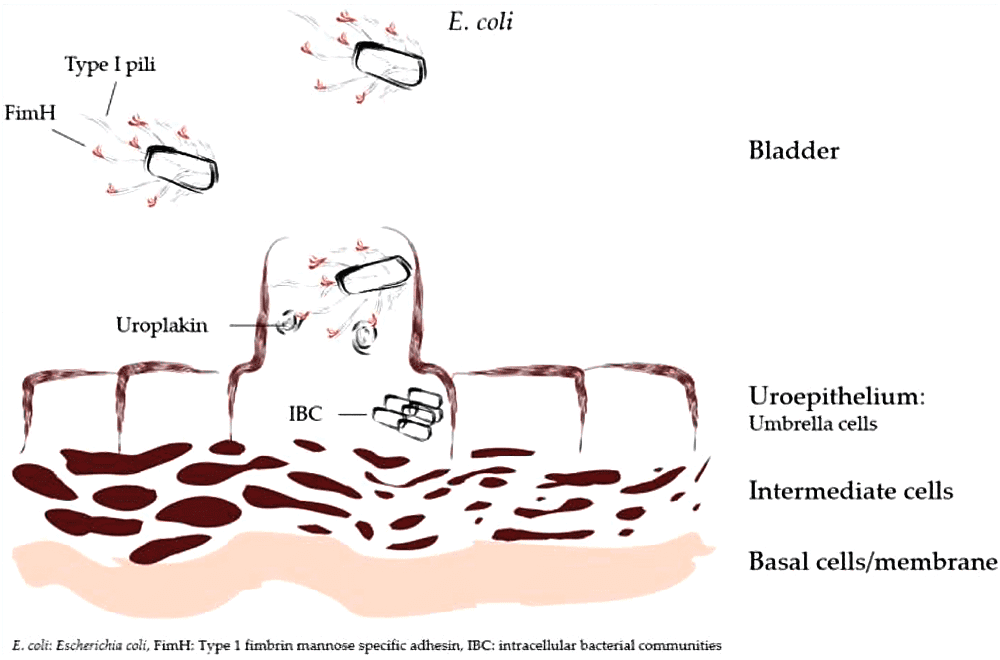
また、膀胱上皮上のウロプラキンと呼ばれる、マンノシル化タンパク質成分に、I型線毛アドへシンのFimH先端を付着させ、その結果シグナルカスケードを活性化してアクチンの再編成を引き起こし、最終的に膀胱上皮細胞を変化させる(umbrella cells)。
膀胱上皮細胞は、生理的に尿で満たされた場合は扁平に、空の収縮した状態では立方形に”移行”することから、移行上皮細胞(transitional epithelial cells)と呼ばれる。この膀胱上皮は、膀胱炎・腎盂腎炎などの炎症や、尿管結石、膀胱癌などの腫瘍、尿道カテーテル挿入や膀胱洗浄といった機械的損傷を受けた場合、umbrella cellsに変化する。
もちろん、UPECが膀胱上皮細胞に作用してこうした変化を起こせば、細胞内の自然免疫系によって認識され、エキソサイトーシスを介して膀胱内に戻され、好中球によって破壊されることになる。しかし、UPECは宿主の免疫系を回避するためにいくつかの戦略を採用していて、細胞内に潜り込んだまま、細胞内バクテリアコミュニティ(IBC)を形成するということが分かってきた。
大腸菌のフィラメント運動を研究したNicholas C. Darntonによれば、個々のべん毛束フィラメントを駆動するモーターは回転方向を頻繁に変更していて、ランダムウォークをしているらしい。べん毛フィラメントは、ユニバーサルジョイントでリバーシブル回転モーターに取り付けられていて、トルクのバランスをとるため、べん毛束は反時計回りに回転し、菌体は時計回りに回転して菌体を前に進めて行く。細菌ごとにこの回転方向の得意、不得意があって、利き手と同様に右回転で上手く進むものと左回転で上手く進むものとが観察されているらしく、大腸菌にも個性があるのだ。
巧妙な仕掛け
David A Rosenらは、膀胱炎マウスモデルで観察された病原性サイクルが、ヒトでも当てはまるかの実証研究を行なった。

上の図は膀胱炎マウスモデルで観察されたUPEC/IBC病原性サイクルだ。Aは正常の膀胱上皮細胞。大きなファセット細胞が並ぶ移行上皮が描かれている。尿路感染性大腸菌(UPEC)が膀胱内に侵入すると、Bの図の如く、先述したように膀胱上皮上のウロプラキンにI型線毛アドへシンのFimH先端を介して、ファセット細胞の表面に付着する。UPECはその後細胞内に侵入し(C)、細胞内で複製を開始する(D)。大腸菌の複製時間は20分だから、あっという間にIBC(細胞内細菌コミュニティ)が作られる。このIBC内では、クオラムセンシングによりバイオフィルムが作られ、UPECはそれに守られてnicheな微小環境で生き延びていく(E)。その後増殖した細菌群は、ファセット細胞を壊して膀胱内に流出し(G)、繊維化(filamentation)を生じて再び病原性サイクルに入っていく。UPECにfilamentationが起こると、細胞は伸長し続けるが分裂はしない状態となる。細胞長が長くなることで、形態的に捕食されにくくなり、好中球の食作用から逃れることが可能となる。また、この現象は抗生物質からの保護にも利用されている。細菌が様々な化学的および物理的な薬剤(例えば、DNA合成阻害抗生物質、紫外線)で処理されると、細菌集団内のフィラメントの数と長さが増加する。ニューキノロン系抗菌薬はこのfilamentationを増長させることで効きにくくなるようだ。こうしたプロセス中に、感染したファセット細胞は尿中に脱落し、好中球が感染部位に動員される(F)。
マウスで確認されたこうしたUPEC/IBC病原性サイクルが、ヒトにも当てはまるのだろうか?
David A Rosenらは、2005年1月から2007年1月の間にワシントン大学(ワシントン州シアトル)学生健康センターで採集された100人(18〜41歳で中央値は22歳)の女性の尿を分析した。80人は合併症のない急性膀胱炎、20人は最近尿路感染を生じたが、今はもう治って症状はない、という人たちだった。大多数は白人(75%)で、未婚(77%)で、55%の女性がサンプル収集の24〜48時間前に性行したと報告した。
詳細については本論文に譲るが、彼らは光学顕微鏡、免疫蛍光と落射蛍光または共焦点レーザー走査顕微鏡、透過型および走査型電子顕微鏡を用いて、サンプル尿中に、IBCを含んだファセット細胞、filamentationを起こしたUPECの存在を検証した。
その結果、マウスで確認されたと同じ所見がヒトでも確認され、同様のサイクルが存在し、UPECは自然免疫から大部分が保護されている可能性が明らかになった。
“which may explain how the relatively few bacteria introduced into the bladder with urethral milking or sexual intercourse are able to survive and multiply to numbers high enough to elicit symptoms in the host.”
「これで、どうして尿道搾尿または性交で、膀胱に入れられた、比較的少数の細菌が、生き残り、十分な数に増殖し、宿主に症状を引き起こすのか、が説明できるかもしれません」
と書かれた論文の締めくくりには多少の違和感がある。欧米女性の活発なsex lifeに大腸菌はむしろ迷惑しているのかもしれないと、そんなことを思ってしまった。
D-Mannoseは効きます!
「STAP細胞はあります!」という言葉が飛び交っていたのは随分前のことだが、今回の執筆で色々と調べた結果は、D-Mannoseは尿路感染症の再発防止に役立つということだった。
多くの文献で示されているのは、膀胱上皮上のウロプラキンにI型線毛アドへシンのFimH先端を介して、UPECが付着するのを防ぐ、ということだ。これにより、UPEC/IBC病原性サイクルの初めの一歩を断つことが出来る。我々臨床医が最も大事にしている、病気を作らない、刀を抜かずに相手を倒す、それが出来る優れものだということだった。
2022年のFabio ParazziniらによるSystematic reviewには、
“In conclusion, despite the limitations, consistent results among all studies give strong support to the general findings. Although the biological and clinical explanations of our results are not entirely clear, observational studies and clinical trials consistently suggest that D-mannose may be useful in the treatment of UTI/cystitis symptoms. Its non-pharmacological, non-metabolic, non-bacteriostatic or bactericidal, but biomechanical mechanism of action, and the fact that it does not affect antibiotic resistance may support the use of D-mannose in the treatment of UTI/cystitis.”
「結論として、限界があるにもかかわらず、すべての研究間で一貫した結果は、一般的な所見を強く支持します。私たちの結果の生物学的および臨床的説明は完全には明らかではありませんが、観察研究と臨床試験は一貫してD-マンノースがUTI/膀胱炎症状の治療に役立つ可能性があることを示唆しています。その非薬理学的、非代謝的、非静菌性または殺菌性ですが、生体力学的作用機序、および抗生物質耐性に影響を与えないという事実は、UTI/膀胱炎の治療におけるD-マンノースの使用を支持する可能性があります」
と結論づけられている。
今回の連載は大変長くなってしまったが、一つの単純な事実の裏にあるscientificなものを確認する、というプロセスを大事にしたからだ。そのための体力、知力がまだ残っていることに感謝して、今後も若い先生方のお役に立てるように精進していきたい。
<資料>
- 1) Jordi van Gestel et.al.:Short-range quorum sensing controls horizontal gene transfer at micron scale in bacterial communities. Nature communications, 2021.:
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2140087/
- 2) 新潟薬科大学「細菌の増殖」:
- https://www2.nupals.ac.jp/~fmfsc/Topics/xi_junno_zeng_zhi.html
- 3) 大腸菌(Wikipedia):
- https://ja.wikipedia.org/wiki/大腸菌
- 4) Maria E. Terlizzi et.al.:UroPathogenic Escherichia coli (UPEC) Infections: Virulence Factors, Bladder Responses, Antibiotic, and Non-antibiotic Antimicrobial Strategies:
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5559502/
- 5) Reeta Ala-Jaakkola et.al.:Role of D-mannose in urinary tract infections – a narrative review:
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8939087/
- 6) えんしんぶんり「移行上皮細胞」:
- https://www.city.fukuoka.med.or.jp/kensa/ensinbunri/enshin_37.pdf
- 7) Nicholas C.Darnton, et.al:On Torque and Tumbling in Swimming Escherichia coli:
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1855780/
- 8) David A. Rosen, et. al:Detection of Intracellular Bacterial Communities in Human Urinary Tract Infection:
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2140087/
- 9) 繊維化(Filamentation)Wikipedia:
- https://ja.wikipedia.org/wiki/繊維化
- 10) Fabio Parazzini et. al.:Systematic review of the effect of D-mannose with or without other drugs in the treatment of symptoms of urinary tract infection/cystitis (Review): Biomedical Reports Aug 17(2); 69,2022.:
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9260159/








